Бертолетова соль или хлорат калия относится к группе кислородосодержащих кислот, ее химическая формула KClO3. На вид это бесцветный порошок, содержащий прозрачные кристаллы, которые легко растворяются в воде. Это взрывоопасное и ядовитое соединение широко применяется в производстве.
Бертолетова соль — это хлорат калия (KClO₃), белое твердое вещество, которое наиболее известно своими окисляющими свойствами и использовалось в производстве спичек и пиротехники.
История
Название “бертолетова” эта соль получила от своего открывателя химика Клода Бертоля. Уроженец Франции впервые получил этот состав в виде белого осадка в ходе своих научных опытов с хлором и гидроксидом калия в 1786 году. Он пропустил хлор через концентрированный горячий щелочной раствор.
2KOH + Cl2 = KCl + KClO + H2O
3KClO = KClO3 + 2KCl
В современном мире эту соль в промышленных масштабах получают с помощью диспропорционирования гипохлоритов, которые получаются при взаимодействии хлора с растворами щелочей. Оформление процесса может быть разным: из-за того, что самый многотоннажный продукт — гипохлорит кальция, из которого состоит хлорная известь, наиболее распространенным процессом является осуществление реакции обмена между хлоратом кальция (он получается при нагревании гипохлорита кальция) и хлоридом калия (он кристаллизуется из маточного раствора). Также хлорат калия получают модифицированным методом Бертолле при бездиафрагменном электролизе хлорида калия, образующиеся при электролизе хлор вступает во взаимодействие в момент выделения с гидроксидом калия с образованием гипохлорита калия, диспропорционирующего далее на хлорат калия и исходный хлорид калия.
Химические свойства
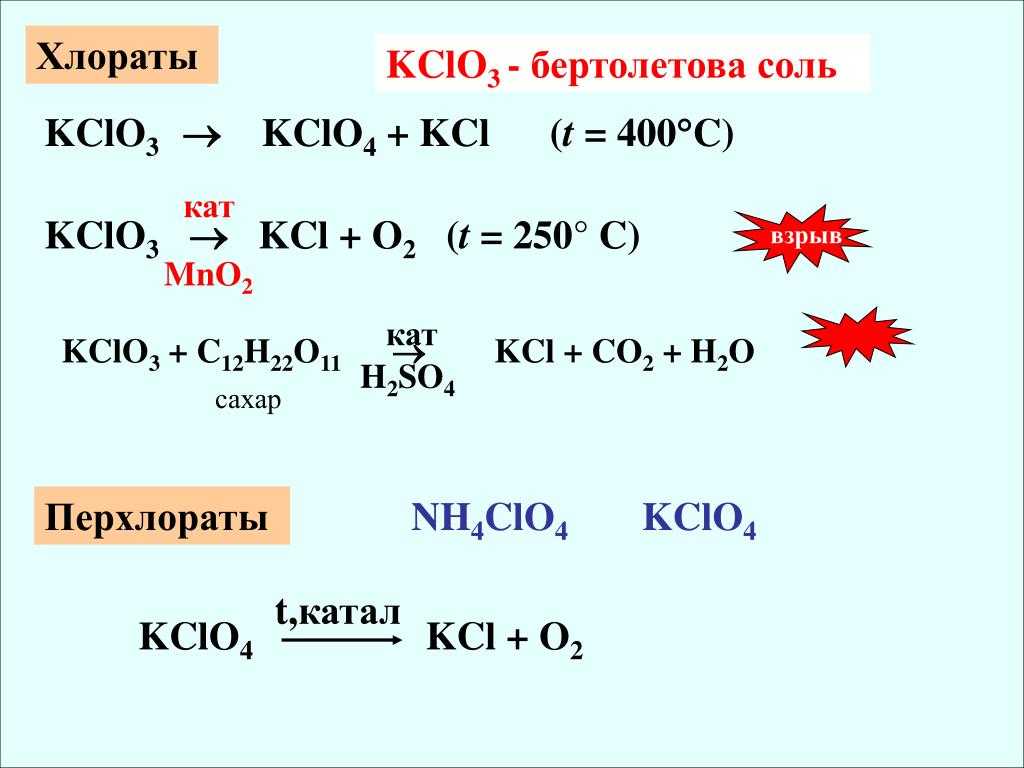
Хлорат калия разлагается при температуре нагревание 400 С°, в результате процесса выделяется кислород и промежуточный перхлорат калия. Если в реакции используются оксиды марганца, железа или меди, то хлористый калий начинает разлагаться при значительно меньшей температуре.
При взаимодействии с сульфатом аммония в спиртовом растворе образовывается неорганическое соединение хлорат аммония, который также обладает взрывоопасным свойством.
Составы, в которые входит этот порошок высокочувствительны, поэтому их редко применяют даже в военной промышленности при производстве. Их можно встретить в сере, используемой для изготовления головок спичек или в некоторых видах пиротехники для получения цветного пламени. И еще реже хлорид калия применятся в качестве взрывчатого вещества в гранатах. Порох с содержанием хлората калия использовали в ручных гранах вермахта. А в Советском Союзе запал для коктейля Молотова в своем составе имел именно эту кислоту, но готовили ее по специальной схеме.
Растворы соли в давние времена могли применять в качестве слабого антисептика, таким “лекарством” полоскали горло. Для получения кислорода раствор стали использовать в начале 20 века, но только в лабораторных условиях. Эксперимент был неудачен из-за высокой чувствительности бертолетовой соли и ее взрывоопасности. Также при помощи нее в лабораторных условиях получают диоксид хлора (проводят реакцию восстановления хлората калия щавелевой и добавляют серную кислоту).
Воздействие на человека
Как и любой другой хлорат, при попадании в организм человека он может привести к тяжелому отравлению, в худшем — к летальному исходу. Степень вреда для людей от этого раствора определяется количеством поступившего яда.
Токсическая доза — 8-10 г, смертельная — 10-30 г.
При попадании внутрь соль превращает гемоглобин в плазму. Эритроциты теряют способность поглощать и доставлять молекулы кислорода к органам и человек задыхается. Время от момента поступления яда в кровь до смерти может занимать от нескольких часов до нескольких дней. При минимальной дозе эритроциты превращаются в студенистую массу, которая закупоривает капилляры, вызывает расстройство мочеотделения, а также тромбозы и закупорку сосудов.
Лечение отравления бертолетовой солью заключается в насыщении крови кислородом и введением внутривенно щелочного физраствора, а также большого количества мочегонных средств. После того, как кровь будет разведена, под кожу вводят раствор пилокарпина для выведения яда со слюной. При коллапсе назначается камфора. При отравлении хлоратом калия строго противопоказаны спирт, его препараты, а также кислые напитки.
Применение
Хлорат калия уже давно применяют в промышленных масштабах в различных сферах жизни. Не только ее взрывоопасные, но и антисептические свойства ценятся при производстве.
Бертолетова соль находит самое широкое применение. Его добавляют в красители, серу для производства спичек и дезинфицирующих средств для обработки поверхностей.
- Военная промышленность. Химические соединения бертолетовой соли и органических соединений и других восстановителей чувствительны к трениям и ударам. При добавлении броматов или сульфата аммония чувствительность возрастает. Подобные смеси используют в военной промышленности при производстве взрывчатых веществ для вооружения.
- Пиротехника. При изготовлении фейерверков также иногда применяется бертолетова соль. Благодаря этому составу при и получается тот самый разноцветный огонь, который можно наблюдать на праздниках.
- Медицина. В медицине его стали использовать как наружный антисептик при заболеваниях горла для полоскания. В настоящем его не используют в качестве лекарственного препарата по причине токсичного воздействия на организм человека. Использования соли для получения кислорода также не имело своего продолжения так как метод очень труднодоступный. KClO3 + C, −2.5mb
- Химическая промышленность. Из бертолетовой соли в промышленных масштабах производят диоксид хлора. Простым языком, та самая “хлорка”, которой хозяйки отбеливают сантехнику в ванной комнате или белое белье. Для получения диоксида хлора.
Безопасность
Данное химическое соединение весьма опасно, поэтому при его использовании, хранении и транспортировки необходимо соблюдать все меры безопасности. Он бурно реагирует, и может самовозгораться или взрываться при смешивании со многими горючими материалами.
Бертолетова соль очень легко воспламеняется при контакте практически с любыми горючими материалами.
Поэтому при любых работах с этим материалом нужно исключить попадание пыли, пуха, опилок и других горючих материалов. Смесь серы, в состав которой входит хлорат калия и пиротехнического состава склонна к самопроизвольному возгоранию, поэтом использование такой серы в фейерверках запрещено. При сочетании топлива с бертолетовой солью и серной кислоты происходит воспламенения состава.
Большая часть серы содержит следовые количества серосодержащих кислот, которые могут вызвать самовозгорание — «Цветы серы» или «возгоночная сера», несмотря на общую высокую чистоту, содержат значительное количество серных кислот. Следует помнить, что готовить смеси такой соли с любым соединением, способствующим воспламенению (одно из таких соединений — сульфид сурьмы (III)) очень опасно, поскольку они чрезвычайно чувствительны к ударам.
Бертолетова соль — опасный и токсичны продукт, при работе с которым нужно соблюдать высокую степень осторожности. Но он находит свое применение в жизни человека в определенных сферах промышленности.